当肺癌患者或家属拿到的基因检测报告结果是阴性的,可能会感到很失望,尤其对晚期肺癌患者,因为他们错过了手术的最佳时机又不想进行化疗。然而,当肺癌患者不能耐受化疗又没有可靶向治疗的基因突变时,可考虑免疫治疗药物。
一、什么是PD-1/PD-L1免疫检查点抑制剂(ICI)?
1、PD-1全称是程序性死亡受体1(programmed death 1)2、PD-L1全称是程序性死亡受体-配体1(programmed celldeath-Ligand 1)3、PD-1/PD-L1免疫抑制剂又称免疫检查点抑制剂,其作用机制:针对PD-1或PD-L1设计特定的蛋白质抗体,PD-1/PD-L1免疫抑制剂阻止PD-1和PD-L1的识别过程,部分恢复T细胞功能,从而使T细胞可以杀死肿瘤细胞。
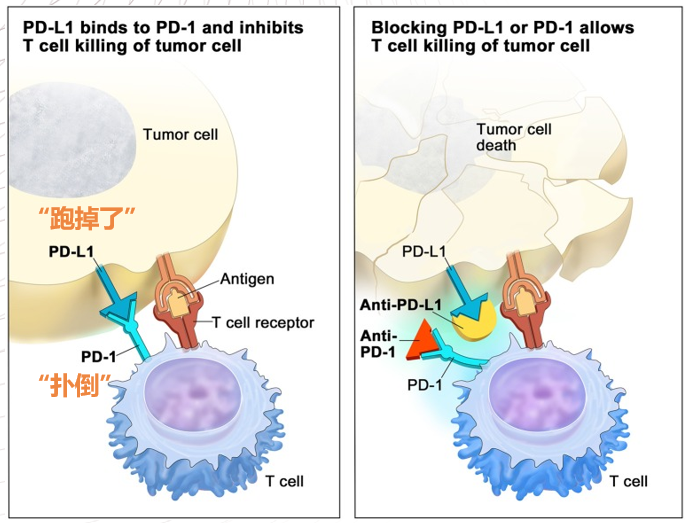
图1

图2中国非小细胞肺癌PD-L1表达检测临床病理专家共识[J]. 中华肿瘤杂志, 2020, 42(7):513-521.
如图2所示:其中有四种免疫药物被FDA获批可用于非小细胞肺癌(NSCLC),分别是纳武利尤单抗(Opdivo,O药)、帕博利珠单抗(Keytruda,K药)、阿替利珠单抗(Tecentriq,T药)和度伐利尤单抗(Imfinzi,I药)。
需注意的是T药和I药还被FDA获批可联合化疗用于广泛期小细胞肺癌的一线治疗。
三、NMPA获批的8种PD-1/PD-L1单抗药物
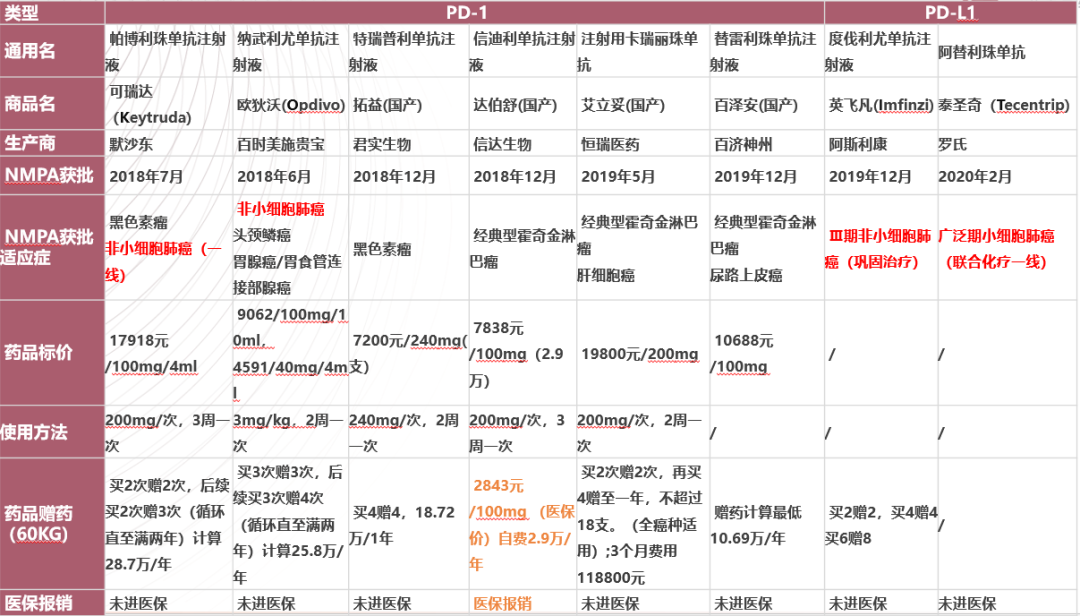
图3
如图3所示:国内上市的8种免疫治疗药物中有6种PD-1单抗药物,2种PD-L1单抗药物。其中,对局部晚期或转移性非小细胞肺癌/广泛期小细胞肺癌、尿路上皮癌、肝细胞癌、经典型霍奇金淋巴瘤、黑色素瘤、头颈鳞癌和胃腺癌/胃食管连接部腺癌共7个癌种均有获批。从上图也可以看出,针对非小细胞肺癌获批的分别是K药、O药和I药。而T药也被国内获批可联合化疗用于广泛期小细胞肺癌的一线治疗。
需注意的是,上图所示的药物价格仅供参考(各地的医保政策各不相同)。
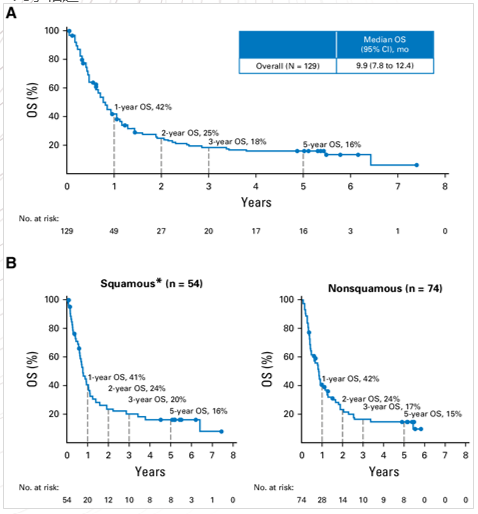
图4
图4是2018年CA209-003研究的5年随访数据:多线治疗失败的晚期肺癌患者使用Nivolumab治疗,5年生存率首次达16%,鳞癌和非鳞癌几乎相近。这与传统的化疗相比,5年生存率显著升高,对晚期肺癌患者无疑是天大的喜讯。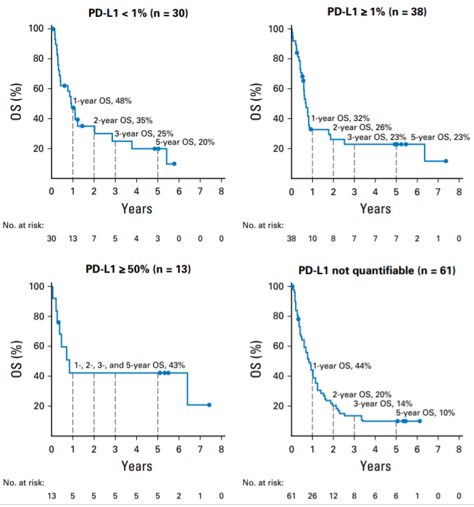
图5
该研究还显示:PD-L1表达越高,生存期越长。其中,PD-L1表达超过50%的13名患者,5年生存率达43%,这意味着接近一半的患者生存期可延长至5年。具体如图5所示。
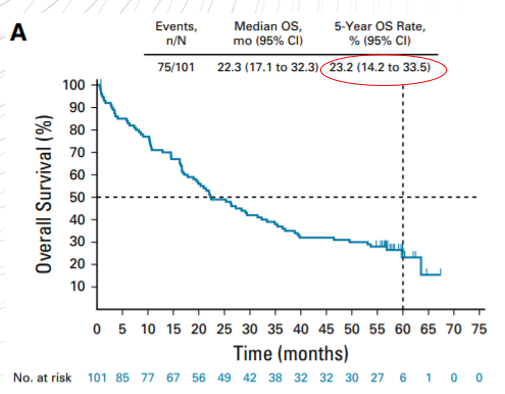
图6 初治患者5年OS
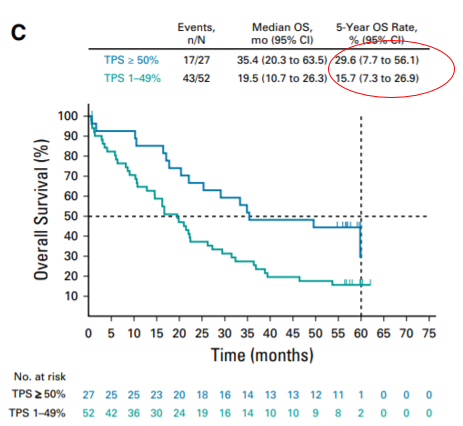
图7 初治患者5年OS(根据PD-L1表达分层)
在另一项KEYNOTE-001(Ib期)研究中,如图6所示,帕博利珠单抗单药一线治疗肿瘤EGFR/ALK均阴性、PD-L1表达≥1%的晚期NSCLC患者,5年生存率为23.2%。从图7中也可以看出,PD-L1表达超过50%的患者,5年生存率为29.6%,显著高于PD-L1低表达的患者。
五、在NSCLC患者中,各国获批的ICI及PD-L1免疫组化检测情况
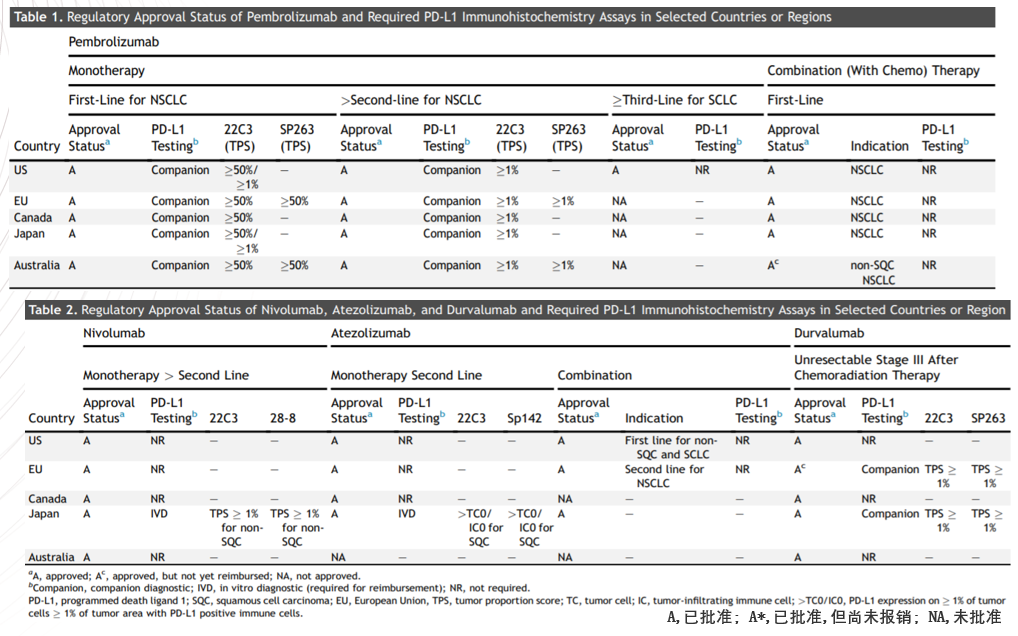
图8
新增:
2020年5月15日,FDA批准O药联合Y药PD-L1表达TPS≥1%且无 EGFR 或 ALK 变异的mNSCLC患者的一线治疗。
2020年5月18日,FDA批准T药PD-L1表达 TC≥50%或IC≥10%且无 EGFR 或 ALK 变异的mNSCLC患者的一线治疗。
图8中,根据各国的获批情况可以看出,共有四种获批的PD-L1抗体用于NSCLC患者,分别是22C3,SP263,22-8和SP142。
六、获批的四种PD-L1 IHC的一致性如何?
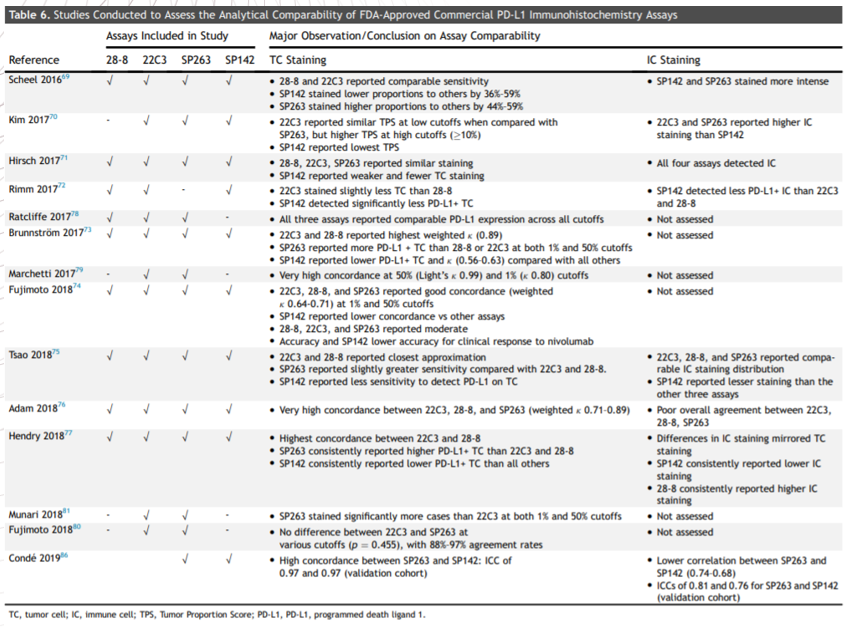
图9
图9中汇总了14项经过临床验证的PD-L1表达染色性能的研究,可以看出22C3、28-8和SP263在肿瘤细胞中表达一致性较好,SP142与22C3、28-8及SP263在肿瘤细胞中表达一致性较差。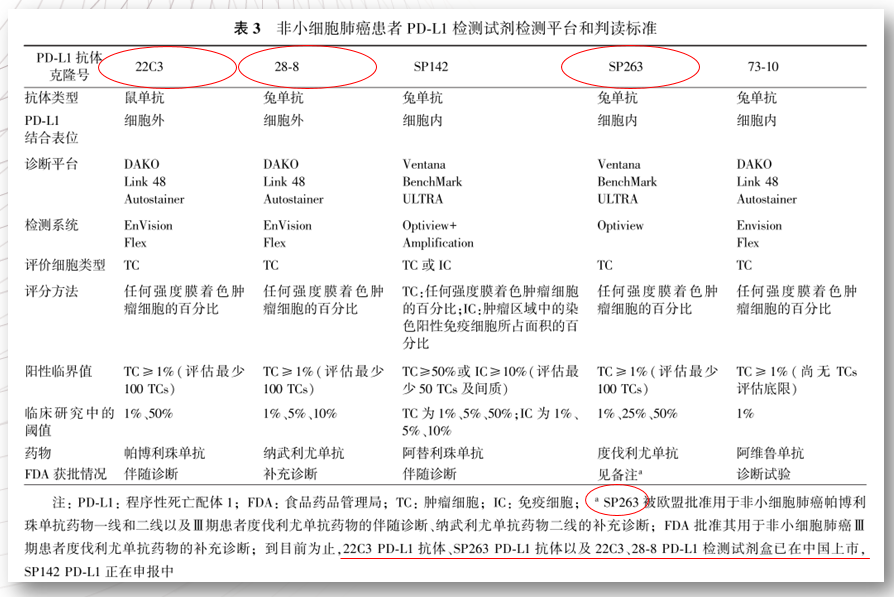
图10 中国非小细胞肺癌PD-L1表达检测临床病理专家共识[J]. 中华肿瘤杂志, 2020, 42(7):513-521.
迄今为止,被NMPA获批的PD-L1抗体分别是22C3、SP263和28-8。从图10中也可以看出,FDA已批准22C3作为帕博利珠单抗的伴随诊断;28-8作为纳武利尤单抗的补充诊断;而SP263被欧盟批准用于非小细胞肺癌帕博利珠单抗药物一线和二线以及Ⅲ期患者度伐利尤单抗药物的伴随诊断、纳武利尤单抗药物的补充诊断,且FDA批准其用于非小细胞肺癌Ⅲ期患者度伐利尤单抗药物的补充诊断。
八、NSCLC PD-L1检测阳性率情况(以22C3为例)
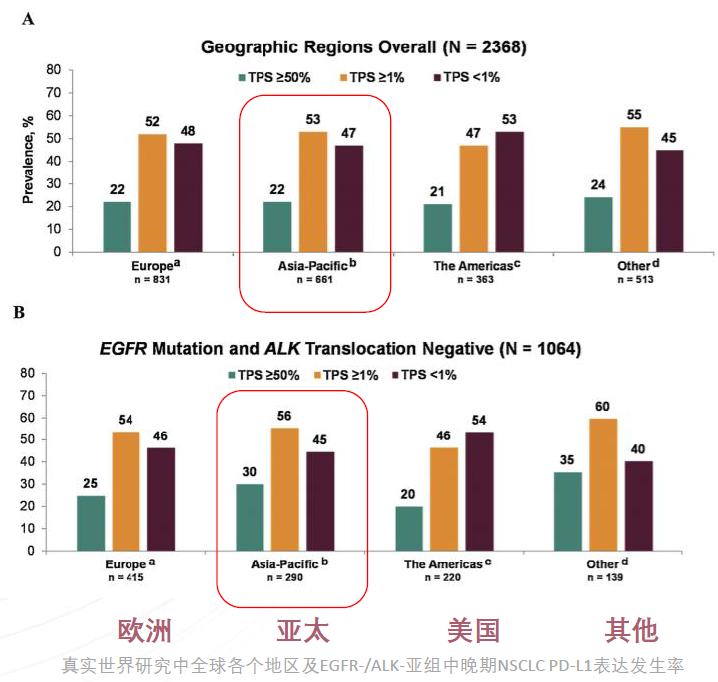
图11
图11所示的研究结果来自于迄今为止使用22C3 pharmDx 试剂盒评估晚期NSCLC PD-L1表达的最大规模(18个国家,45个中心)估计真实世界的研究。可以看出,晚期NSCLC患者的PD-L1 TPS≥50%和TPS≥1%在全球各个地区的发生率相似。以亚太人群为例,A图中,TPS≥50%的发生率为22%,TPS≥1%的发生率为53%;而B图中分析了EGFR-/ALK-亚组中晚期NSCLC PD-L1表达发生率,其中高表达的为30%,低表达的为56%,与未筛选驱动基因组相比略有升高。九、NMPA:PD-L1表达+EGFR+ALK检测是K药单药一线治疗前提
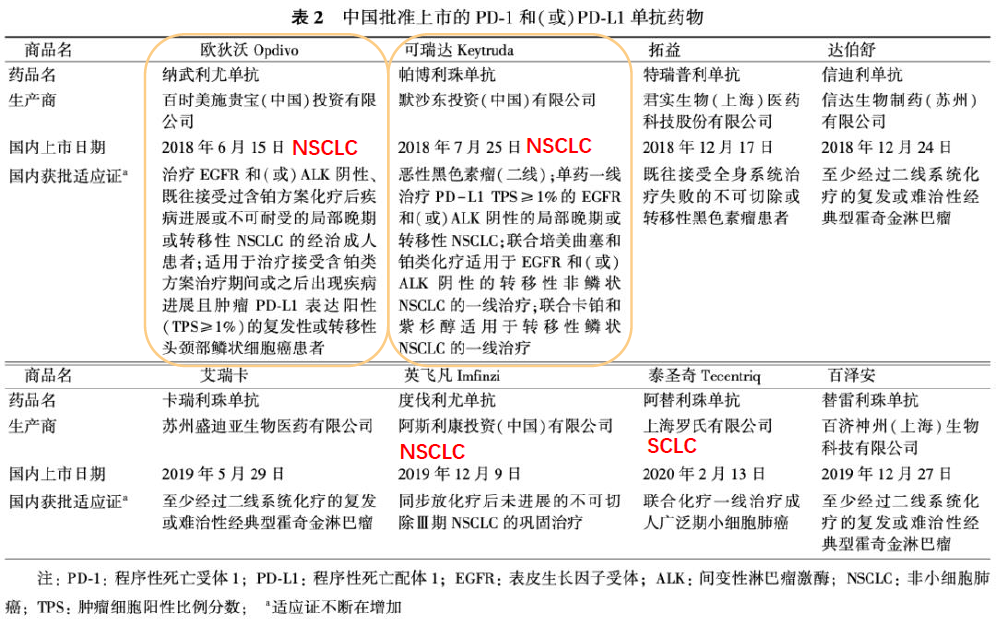
图12 中国非小细胞肺癌PD-L1表达检测临床病理专家共识[J]. 中华肿瘤杂志, 2020, 42(7):513-521.
回到上文第三点中提到的,NMPA共获批的8种PD-1/PD-L1单抗药物中有3种适用于NSCLC。在图12中可以看出,EGFR阴性和(或)ALK阴性、PD-L1表达阳性(TPS≥1%)是帕博利珠单抗作为单药一线治疗局部晚期或转移性NSCLC的前提,这与本文的主旨“NSCLC患者驱动基因阴性,更要做PD-L1检测”相呼应。
十、CSCO指南:无驱动基因突变是ICI治疗非鳞非小细胞肺癌前提
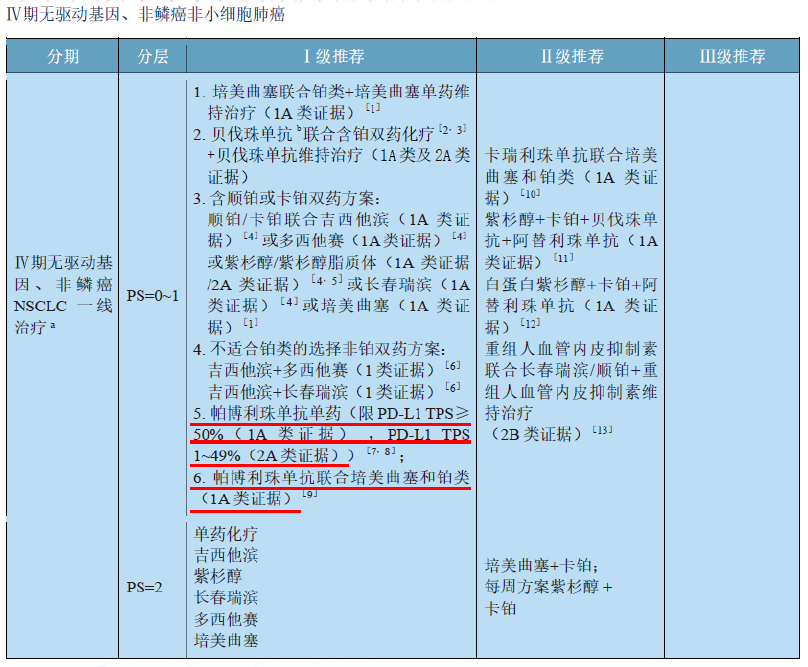
图13 2020 CSCO非小细胞肺癌诊疗指南
在CSCO指南中,针对Ⅳ期无驱动基因、非鳞癌非小细胞肺癌的一线治疗,也指出了免疫治疗。其中Ⅰ级推荐中:1、上调帕博利珠单抗单药一线治疗(限PD-L1TPS≥50%)为Ⅰ级推荐(1A类证据)。这是基于KEYNOTE-024研究2019年更新结果:帕博利珠单抗组和化疗组的mOS分别为30个月和14.2个月(HR=0.63),24个月的总生存率分别为51.5%和34.5%。
2、新增帕博利珠单抗单药一线治疗(限PD-L1TPS 1~49%)(2A类证据)。这是基于2019年公布的KEYNOTE-042中国研究结果,在PD-L1 TPS≥50%人群中,两组中位OS期分别为20.0个月和14.0个月(HR=0.62);在PD-L1 TPS=1~49%人群中,帕博利珠单抗组同样显著优于化疗组,两组mOS分别为19.9个月和10.7个月(HR=0.69)。3、上调帕博利珠单抗联合培美曲塞和铂类(1A类证据)至Ⅰ级推荐。根据KEYNOTE-189:无论PD-L1表达水平如何,帕博利珠单抗联合培美曲塞/铂类组和安慰剂联合培美曲塞/铂类组的更新mOS分别为22.0个月和10.7个月(HR 0.56)。帕博利珠单抗联合组和安慰剂联合组的中位PFS分别为9.0个月和4.9个月(HR 0.48)。十一、CSCO指南:无驱动基因突变是ICI治疗鳞癌前提
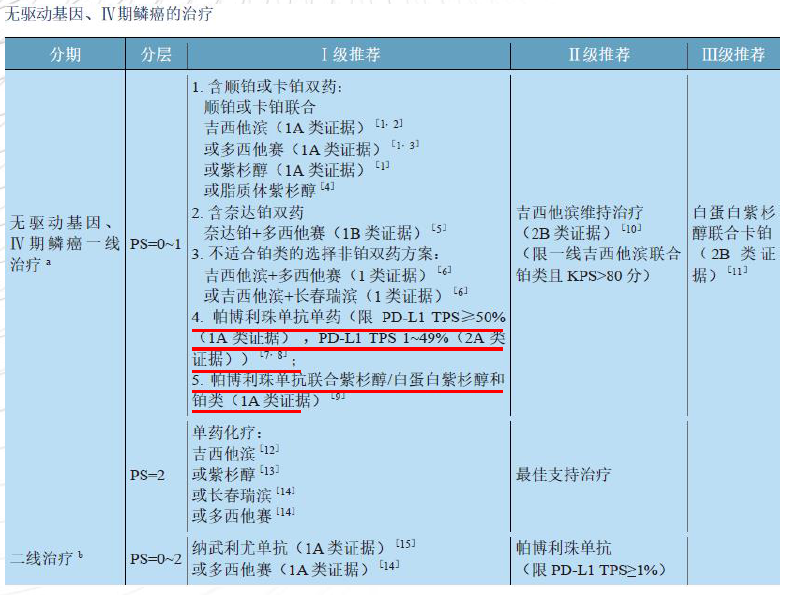
图14 2020 CSCO非小细胞肺癌诊疗指南
其中帕博利珠单抗单药的用药依据与上文中的非鳞癌非小细胞肺癌相同,都是根据KEYNOTE-024和KEYNOTE-042的研究结果。而关于免疫治疗联合化疗则是上调了帕博利珠单抗联合培美曲塞和铂类(1A类证据)至Ⅰ级推荐。根据KEYNOTE-189:无论PD-L1表达水平如何,帕博利珠单抗联合培美曲塞/铂类组和安慰剂联合培美曲塞/铂类组的更新mOS分别为22.0个月和10.7个月(HR 0.56)。帕博利珠单抗联合组和安慰剂联合组的中位PFS分别为9.0个月和4.9个月(HR 0.48)。十二、专家共识:无驱动基因突变是ICI治疗非小细胞肺癌前提
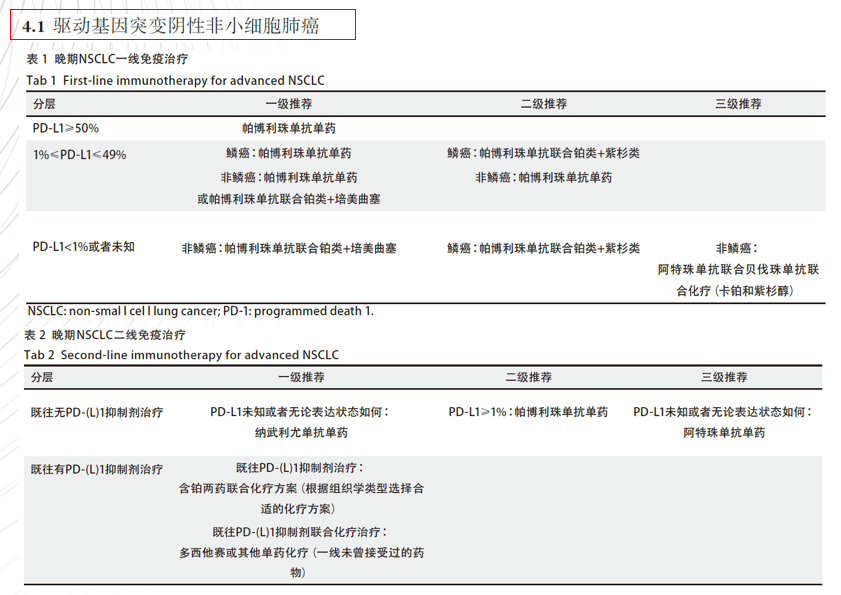
图15来源中国临床肿瘤学会(CSCO)NSCLC专家委员会组织相关专家共同制定的《中国非小细胞肺癌免疫检查点抑制剂治疗专家共识(2019年版)》
图15是关于驱动基因突变阴性的晚期非小细胞肺癌的一线、二线免疫治疗的汇总。在一线治疗的一级推荐中,如果PD-L1表达,可以使用K药单药治疗;如果PD-L1<1%或者未知,对于非鳞癌患者,可以使用K药联合铂类+培美曲塞。而对二线治疗的一级推荐,则没有指出需要做PD-L1抗体表达检测。
十三、NSCLC驱动基因阳性应首选靶向药物(KRAS除外)
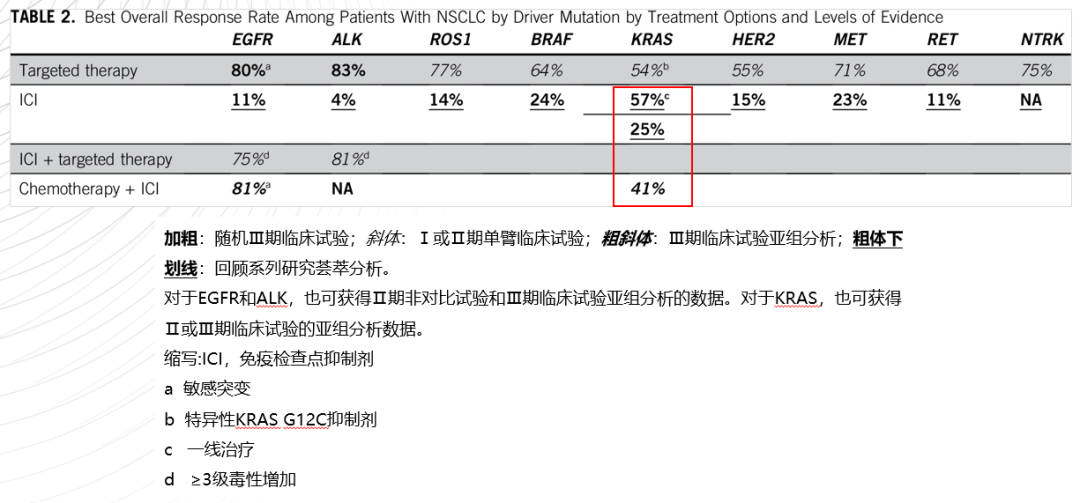
图16
从图16可以看出,对于NSCLC患者,如果驱动基因发生突变(KRAS除外),使用靶向治疗的ORR高于免疫治疗,尤其是对于EGFR和ALK更为明显。而对于KRAS这个特殊基因,接下来会有所介绍。
十四、NCCN指南关于KRAS基因的说明

图19
NCCN指南中指出:KRAS癌基因是一种预后生物标志物。KRAS突变的NSCLC患者与无KRAS突变的患者相比生存期短,是独立于治疗以外的预后因素。KRAS突变也预示着患者不能从EGFR-TKI治疗中获益。虽然免疫治疗似乎是有效的,但是靶向药物目前不可用。
十五、PD-L1检测样本类型注意事项

图20 中国非小细胞肺癌PD-L1表达检测临床病理专家共识[J]. 中华肿瘤杂志, 2020, 42(7):513-521.
具体详细内容,可以看往期推文:
凡事预则立,送检流程需规范!
我司绘真医学也可提供NSCLC患者使用免疫治疗的检测项目,具体如下表所示。小编在这边还想强调一下,我司的实体瘤196基因检测将在9月20日之后升级优化为实体瘤201基因,有关实体瘤201基因的详细介绍,可以看往期推文:
1、J.Clin. Oncol. 2018 06 10;3617(17)2、J.Clin. Oncol. 2019 10 01;3728(28)3、Journalof Thoracic Oncology Vol. 15 No. 4: 499-5194、Journalof Thoracic Oncology Vol. 15 No. 4: 499-519






