快讯|FDA批准Olaparib+Bevacizumab用于HRD+ 卵巢癌的一线维持疗法
奥拉帕尼(olaparib)是多聚二磷酸腺苷核糖聚合酶(PARP)抑制剂,抑制PARP1/2/3。在体外研究中,奥拉帕尼抑制PARP活性和PARP-DNA结合物形式的增加,增加双链DNA的断裂,导致BRCA基因突变失活的癌细胞DNA无法修复、有丝分裂被破坏、细胞死亡。
商品名:Lynparza
药品名:Olaparib
中文名:奥拉帕尼
生产商:阿斯利康、默沙东
推荐剂量:每日两次,每次400mg
2020年5月8日FDA批准了奥拉帕尼(olaparib,Lynparza)和贝伐单抗(bevacizumab,Avastin)组合作为维持疗法,治疗一线含铂化疗+贝伐单抗治疗后完全缓解(CR)或部分缓解(PR)的晚期同源重组缺陷(HRD)阳性卵巢癌患者。 ( HRD被定义为BRCA有害或疑似有害突变,和/或基因组不稳定 )。 [1]

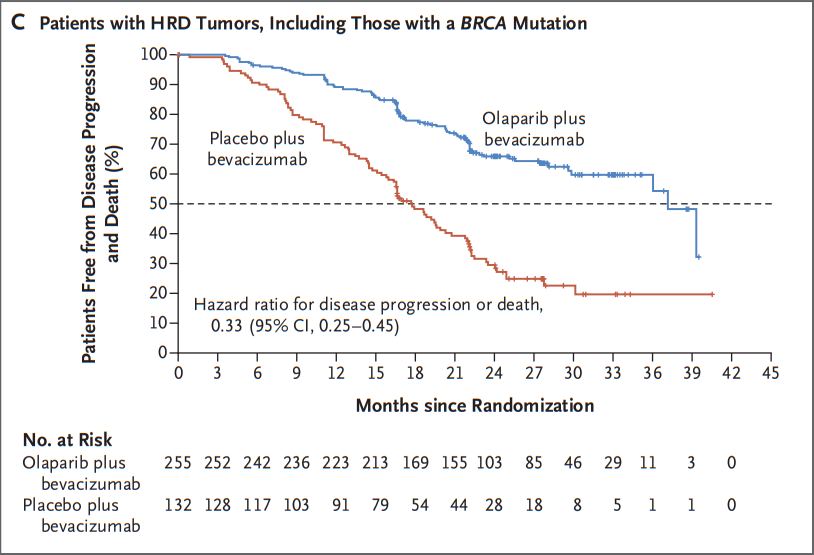
这项批准基于关键的3期PAOLA-1试验结果,与单独使用贝伐单抗相比,该组合降低了疾病进展或死亡的风险。在HRD阳性肿瘤(包括携带BRCA突变的肿瘤)患者中,加入奥拉帕尼的获益最为明显(HR,0.33; 95%CI,0.25-0.45)。在该亚组中,奥拉帕尼+贝伐单抗联合用药组和单药贝伐单抗组的中位无进展生存期(PFS)分别为37.2个月和17.7个月。
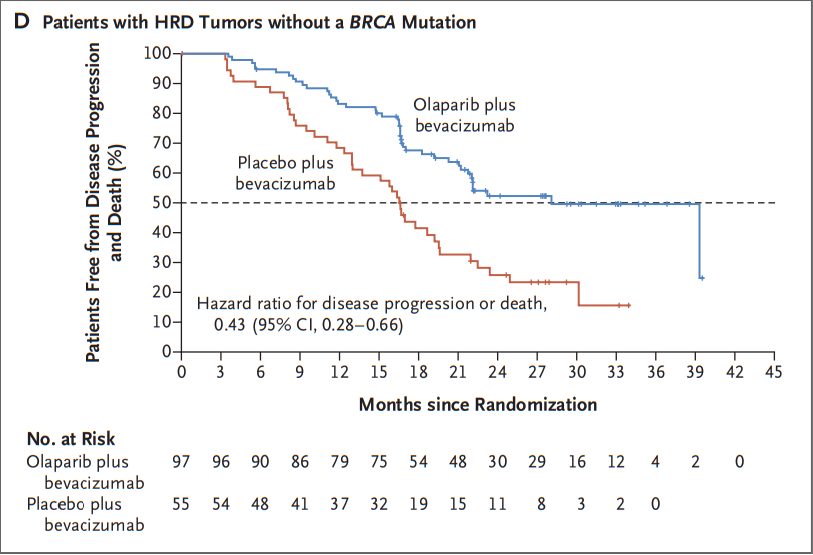
在不携带BRCA突变的HRD阳性肿瘤患者中,奥拉帕尼+贝伐单抗联合用药组与单药贝伐单抗组的中位PFS分别为 28.1个月 和16.6个月( HR,0.43;95%CI,0.28-0.66 )。
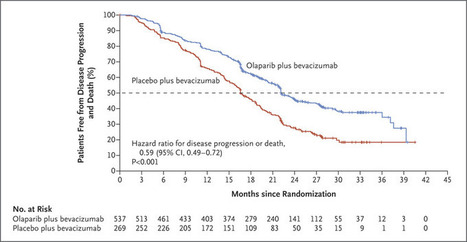
在ITT(意向治疗)人群中,与单独使用贝伐单抗相比,研究者评估该组合降低了41%的疾病进展或死亡风险(HR,0.59;95%CI,0.49-0.72;P <.001)。此外,在中位随访22.9个月后,单独使用贝伐单抗和联合使用贝伐单抗的中位PFS分别为22.1个月和16.6个月。
“卵巢癌是一种破坏性疾病。在PAOLA-1试验中,该组合用药为HRD阳性患者带了重要获益。我期待它进入临床实践,”法国克劳德伯纳德里昂第一大学PAOLA-1试验首席研究员兼医学肿瘤学家Isabelle Ray-Coquard博士说。 [2]
在双盲,安慰剂对照的3期PAOLA-1试验中,新诊断、晚期、FIGO III至IV期、高级别、浆液性或子宫内膜样卵巢癌、输卵管癌或腹膜癌患者( 经一线含铂化疗和贝伐单抗的治疗CR或PR,无论其基因生物标志物的突变状态或预先手术的结果如何 )以2:1的比例随机接受奥拉帕尼联合贝伐单抗( n = 537 )或贝伐单抗联合安慰剂( n = 269 )作为一线维持治疗。每3周以15 mg / kg的剂量使用贝伐单抗;在实验组中,每日两次服用300mg奥拉帕尼。不论手术的类型或程度招募患者。患者中位年龄为60.5岁,ECOG表现状态均为0或1。主要终点是研究者评估的PFS。次要终点包括PFS2,总生存期( OS ),首次接受治疗或死亡的时间,以及欧洲癌症研究和治疗组织研制的生活质量问卷。
关于安全性,联合用药组与单独使用贝伐单抗组相比,在≥20%的患者中发生的最常见不良反应(AE)为疲劳(53%vs.32%),恶心(53%vs.22%),高血压(46%vs.60%),贫血(41%vs.10%),淋巴细胞减少症(24%vs.9%),呕吐(22%vs.11%)和关节痛(22%vs.24%)。
据报道,接受奥拉帕尼+贝伐单抗治疗的患者中有57%的AE≥3 级,而仅接受贝伐单抗治疗的患者中有51%发生了至少3级AE。这些AE包括高血压(19%vs.30%),贫血(17%vs.<1%),淋巴细胞减少症(7%vs.1%),疲劳(5%vs.1%),中性白细胞减少症(6%vs.3%),恶心(2%vs.1%),腹泻(均为2%),白细胞减少症(2%vs.1%),呕吐(1%vs.2%)和腹痛(1%vs.2%)。
奥拉帕尼+贝伐单抗的患者组中有54%的患者发生了导致剂量中断的AE,单药贝伐单抗组中有24%。两组发生剂量减少的AE分别为41%和7%。联合用药的患者中有20%中止治疗,而单药贝伐单抗组为6%。
2014年12月,FDA批准第一个PARP抑制剂奥拉帕尼用于之前至少经过3次化疗,携带BRCA基因突变的卵巢癌患者的单药治疗。
2017年8月,FDA批准奥拉帕尼用于接受含铂化疗后CR或PR的复发性上皮性卵巢癌,输卵管癌或原发性腹膜癌成年患者的单药维持治疗。
2018年12月,FDA批准奥拉帕尼作为维持疗法,治疗一线含铂化疗后CR或PR,携带BRCA有害或疑似有害胚系或体系突变的晚期上皮性卵巢癌,输卵管癌或原发性腹膜癌患者。该批准基于3期SOLO-1试验的结果,在该试验中,奥拉帕尼降低了70%的疾病进展或死亡风险(与含铂化疗后接受安慰剂治疗相比,HR,0.30;95%CI,0.23-0.41;P <.001)。[3]
参考文献:
1.Highlights of olaparib (Lynparza) prescribing information. FDA. Updated May 8, 2020. https://bit.ly/2Wfjsgz. Accessed May 8, 2020
2.LYNPARZA® (olaparib) Approved by FDA as First-Line Maintenance Treatment with Bevacizumab for HRD-Positive Advanced Ovarian Cancer. Published May 8, 2020. https://bit.ly/3cft3tu. Accessed May 8, 2020.
3.Moore K, Colombo N, Scambia G, et al. Maintenance olaparib in patients with newly diagnosed advanced ovarian cancer. N Eng J Med. 2018;379(26):2495-2505. doi: 10.1056/NEJMoa1810858